mRNA 치료 새 단초 마련…사이언스誌 게재
|
과학기술정보통신부는 기초과학연구원(IBS) RNA 연구단 김빛내리 단장 연구진이 mRNA 백신의 세포 내 전달과 분해를 제어하는 단백질 군을 찾아내고 그 작동원리를 최초로 규명했다고 3일 밝혔다. 이번 연구 결과는 세계 최고 권위 학술지 사이언스에 4일 온라인 게재됐다.
코로나19 백신으로 대표되는 mRNA 기반 기술은 감염병 대응뿐 아니라 암 백신, 면역 및 유전자 치료 등 다양한 활용이 가능한 점이 특징이다. 그러나 치료용 RNA가 체내에서 어떻게 작동·조절되는지 구체적인 기작은 충분히 알려지지 않았다. 또한 코로나19 백신의 주역인 N1-메틸수도유리딘 변형 염기는 mRNA 백신의 효능 혁신과 상용화를 이끌었지만 무엇이 효능을 높였는지, 원리가 무엇인지는 분명치 않았다.
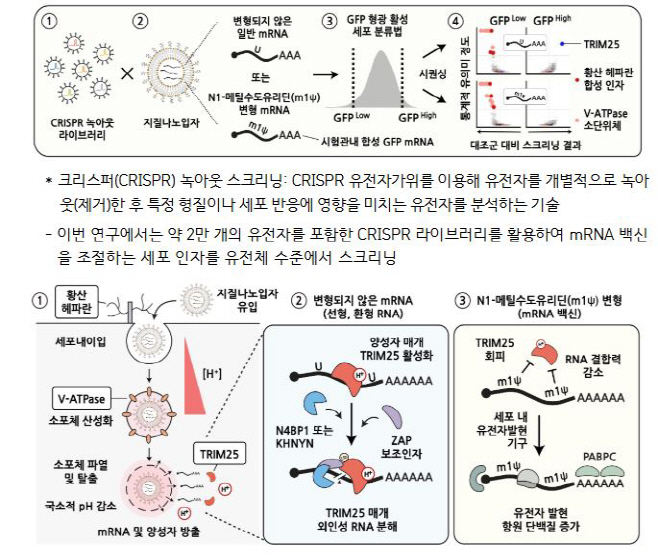
이에 IBS 연구진은 mRNA를 제어하는 세포 내 인자들을 찾아내고자 유전자가위를 이용한 녹아웃 스크리닝을 면밀하게 진행했다. mRNA 치료제의 효능을 높이고 부작용을 없애려면 mRNA가 세포로 유입·조절되는 인자와 활용되는 과정을 이해해야 가능하기 때문이다.
그 결과, 연구진은 발견 mRNA가 세포 내로 전달·유입되는 데 필요한 핵심 단백질 인자들과 조절 경로를 밝혀냈다.
구체적으로 살펴보면 우선, 세포막 표면에 있는 '황산 헤파란' 분자는 mRNA를 감싼 지질나노입자와 결합해 세포 내 유입을 촉진한다. 이를 통해 지질나노입자는 세포내 소포체로 들어가게 된다.
양성자 이온 펌프 'V-ATPase'는 소포체 내부를 산성화시키고 지질나노입자가 양전하를 띄도록 해 소포체 막을 일시적으로 파열시키는데, 이 막이 깨지면서 mRNA가 세포질로 방출, 단백질로 발현할 수 있게 되는 것이다.
연구진은 발견 RNA 치료제에 대한 주요 억제 인자와 함께 외부 RNA의 침입을 경보하는 양성자 이온의 중요한 역할도 최초로 발견했다.
세포질 내 'TRIM25' 단백질이 mRNA를 침입자로 인식하고 제거한다. 이 단백질은 소포체 막이 파열되면서 방출되는 양성자 이온에 의해 활성화되며, 외인성 RNA에 특이적으로 표적·결합해 다른 절단 효소 및 보조 단백질과 함께 RNA를 빠르게 절단하고 분해한다.
아울러 연구진은 발견 mRNA를 결합·제거하는 TRIM25 단백질이 N1-메틸수도유리딘 변형 염기에는 그 결합력이 현저히 감소, mRNA를 절단·분해하지 못한다는 사실도 발견했다. 코로나19 mRNA 백신의 효능과 안정성을 향상시킬 수 있었던 요인과 원리를 이해하게 된 것이다.
과기부 관계자는 "이번 연구는 mRNA 백신의 세포 내 작동 원리를 최초로 밝혀냄으로써 mRNA 치료제의 효능과 안정성을 한 단계 높여갈 이론적 토대가 마련됐다는데 큰 의미가 있다"고 말했다.
김빛내리 단장은 "양성자 이온이 면역 신호 전달 물질로 작용한다는 사실을 최초로 발견하고 외부 침입자에 대항하는 세포의 방어 기전에 대한 이해를 한층 넓혀 RNA뿐 아니라 면역, 세포신호 분야에도 새로운 연구 방향을 제시할 것으로 보인다"고 전했다.